Laboratorio Bradfute

Enfermedades infecciosas / patógenos como aquellos que han aparecido recientemente en una población o han existido pero están aumentando rápidamente en incidencia o rango geográfico.

El ratón ciervo Peromyscus maniculatus es portador del hantavirus Sin Nombre, que es responsable de la mayoría de los casos de síndrome cardiopulmonar por hantavirus en los EE. UU.
Crédito de la foto: Sam Goodfellow

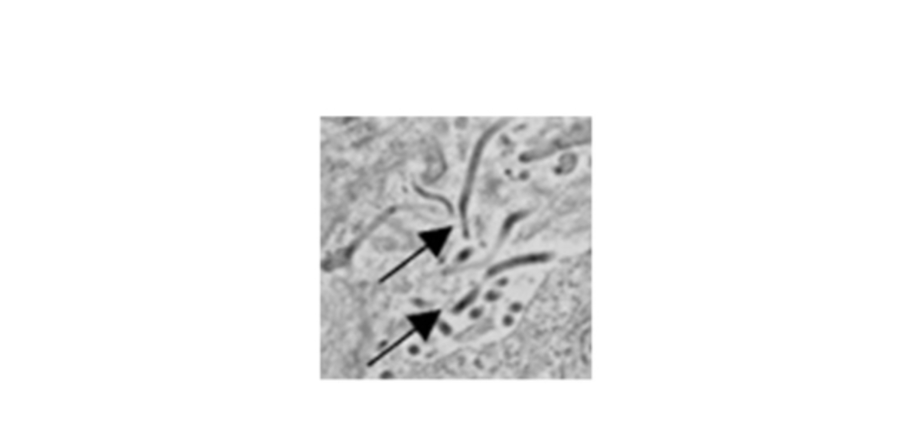
Virus del Ébola en bazo infectado. Las flechas apuntan a viriones individuales. Imágenes realizadas mediante microscopía electrónica de transmisión.
Crédito de la foto: Steven Bradfute, PhD

Ensayo de placa del virus del Zika para identificar anticuerpos neutralizantes
Crédito de la foto: Steven Bradfute, PhD
La infección por el virus del Ébola provoca la muerte de las células inmunitarias. La microscopía de fluorescencia muestra las células del bazo de un animal infectado. El rojo marca las células moribundas y muestra todas las células.
Crédito de la foto: Steven Bradfute, PhD
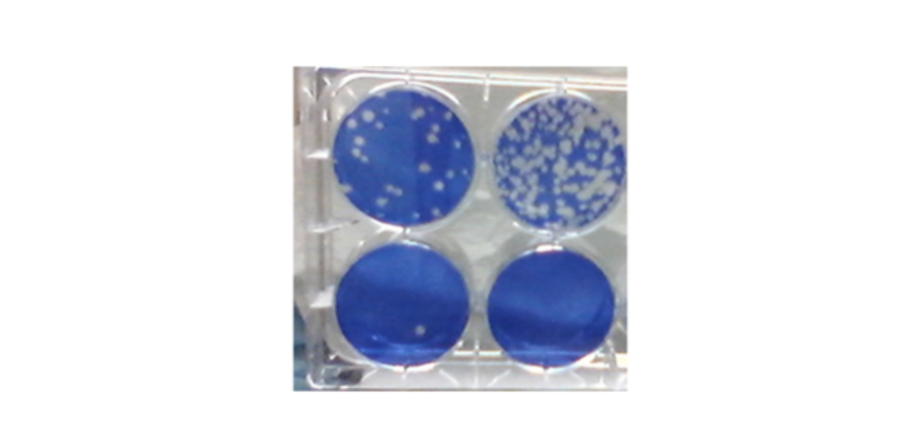
Ensayo de placa SARS-CoV-2 para medir la inhibición de la replicación del coronavirus. El color azul son células vivas; Los agujeros son "placas que muestran dónde el SARS-CoV-2 ha infectado y destruido las células.
Crédito de la foto: Steven Bradfute, PhD
Los hantavirus son patógenos peligrosos que causan enfermedades graves en los seres humanos. Los virus se replican de forma inofensiva en roedores y se transmiten a los seres humanos por inhalación de virus en excrementos de roedores en aerosol. El primer hantavirus patógeno en los EE. UU., El hantavirus Sin Nombre, fue descubierto en Nuevo México en 1993. Nuevo México ha tenido la mayor cantidad de casos de hantavirus Sin Nombre que cualquier otro estado, lo que lo convierte en un virus importante para nuestra región, especialmente dada su alta letalidad. tasa en humanos (~ 35%). Nuestra investigación cubre múltiples áreas de la biología y la terapéutica del hantavirus.
-Anticuerpos neutralizantes para terapéutica.
Tenemos un esfuerzo de colaboración como parte de una subvención NIH U19 basada en la Facultad de Medicina Albert Einstein para identificar y analizar anticuerpos monoclonales contra múltiples hantavirus. El consorcio utiliza estos datos para seleccionar anticuerpos para probar su capacidad para rescatar de la infección a modelos de animales pequeños. Este estudio colaborativo se destaca en el podcast "This Week in Virology": https://www.microbe.tv/twiv/twiv-578/
--Respuestas inmunes de memoria a largo plazo en supervivientes del hantavirus Sin Nombre.
Estamos rastreando las respuestas inmunes a largo plazo en los sobrevivientes del hantavirus Sin Nombre. Hasta la fecha, hemos encontrado respuestas de anticuerpos muy fuertes en los supervivientes, con pacientes hasta 23 después de la infección que todavía muestran respuestas de anticuerpos neutralizantes detectables. Estos datos sugieren que los supervivientes de hantavirus generan una inmunidad fuerte y duradera contra la reinfección. También hemos establecido un ensayo de citometría de flujo de 13 colores para probar respuestas específicas de recuperación de hantavirus en múltiples compartimentos de células T CD8 + y CD4 + de memoria.
--Análisis genético del virus Sin Nombre en roedores capturados en la naturaleza en Nuevo México.
El roedor huésped del hantavirus Sin Nombre es el ratón ciervo Peromyscus maniculatus. Los ratones ciervo tienen un rango natural muy extenso, ya que se encuentran en casi todos los Estados Unidos (excluyendo las regiones del sureste). Sin embargo, la infección por el virus Sin Nombre en humanos se concentra principalmente en el oeste y suroeste de EE. UU. Hacemos la pregunta "¿por qué los ratones ciervo están en todas partes pero los humanos infectados no?" Estamos respondiendo a esta pregunta atrapando ratones ciervos salvajes en todo Nuevo México, tanto en regiones endémicas de infección humana como no endémicas, para determinar si a) el virus Sin Nombre solo se encuentra en regiones endémicas de pacientes humanos ob) la secuencia del genoma del virus es significativamente diferente en diferentes regiones.

El laboratorio de Bradfute aprovechó nuestra experiencia en patógenos virales emergentes para estudiar el virus del Zika durante el brote de 2013-2016. Colaboramos con Los Alamos National Laboratories para probar la eficacia de un nuevo sistema de administración de ADN / nanopartículas para proteger a los ratones de la infección por el virus del Zika. Descubrimos que una vacuna de ADN plasmídico formulada en un sistema de administración novedoso inducía inmunidad protectora contra la infección por el virus del Zika en ratones de una manera dependiente de la dosis.
Hraber P, Bradfute SB, Clarke E, Ye C y Pitard B. Suministro de copolímero de bloque anfifílico de una vacuna de ADN contra el virus del Zika. Vacuna 36: 6911 (2018)

El laboratorio de Bradfute participa en la prueba de nuevas vacunas para la inducción de respuestas inmunitarias de reacción cruzada contra múltiples virus de encefalitis, que son transmitidos por mosquitos y causan enfermedades graves tanto en caballos como en humanos.
- Suministro de antígeno nanoportador para vacunas de alfavirus de dosis única de protección amplia.
Nos estamos asociando con Los Alamos National Laboratories (LANL) para probar una nueva vacuna basada en ADN para proporcionar inmunidad duradera de una sola inyección contra múltiples alfavirus. Nuestro papel en esta colaboración es probar vacunas de ADN para su inducción de respuestas de anticuerpos y células T en ratones, utilizando alfavirus BSL-3 como objetivos.
- ARN largos no codificantes en la infección por el virus de la encefalitis equina venezolana.
Recientemente hemos recibido una subvención para un gran proyecto que estudia el papel de los ARN largos no codificantes en las respuestas celulares a la infección por el virus de la encefalitis equina venezolana. Este proyecto aprovechará nuestras instalaciones de agente selecto BSL-3 en UNM HSC para probar qué ARN largos no codificantes se expresan después de una infección in vitro e in vivo de un virus patógeno de encefalitis equina venezolana en comparación con una versión no patógena del mismo virus. De esta manera, podremos comparar directamente qué ARN largos no codificantes se inducen o suprimen en una respuesta celular exitosa frente a una respuesta fallida.
El virus del Ébola es un patógeno mortal que tiene una tasa de mortalidad de más del 40%. Aunque tradicionalmente se limita a pequeños brotes en aldeas aisladas, el virus comenzó a extenderse a las grandes ciudades por primera vez, provocando un brote mundial entre 2013 y 2016. Estamos involucrados en esfuerzos para el desarrollo de vacunas y terapias para este virus.
-Desarrollo de vacunas y terapias contra el virus del Ébola.
Descubrimos que los cambios de glicosilación (patrón de azúcar) en la glicoproteína viral afectan dramáticamente la forma en que estas proteínas inducen una respuesta inmune cuando se usan como vacuna. Estos cambios en la glicosilación ocurren cuando las vacunas se fabrican en diferentes tipos de células. Nuestros hallazgos fueron relevantes, ya que se utilizan diferentes tipos de células para diferentes vacunas.
-Administración terapéutica y conjunta de vacunas contra el virus del Ébola.
Nuestros estudios sobre el virus del Ébola han continuado con la financiación reciente de una segunda subvención, en la que estamos estudiando cómo la administración de terapias a corto plazo junto con las vacunas a largo plazo afecta la eficacia de estos tratamientos. El objetivo es determinar el momento óptimo para administrar ambos fármacos terapéuticos para una protección inmediata contra el virus sin derogar la protección a largo plazo de las vacunas coadministradas.

Dada la urgencia de la pandemia de coronavirus en curso, el laboratorio Bradfute encabezó el trabajo del virus BSL-3 SARS-CoV-2 en UNM HSC. Hemos colaborado con más de 25 grupos académicos y comerciales diferentes para utilizar nuestra especialización única en la investigación de terapias, vacunas, inactivación, biología básica y análisis de muestras de pacientes para el SARS-CoV-2.
- Evaluación de anticuerpos neutralizantes en pacientes convalecientes y agudos COVID-19.
El laboratorio de Bradfute probó títulos de anticuerpos neutralizantes en plasma de individuos convalecientes y plasma de pacientes con COVID-19 agudo que habían sido infundidos con plasma convaleciente como terapia experimental en UNMH. Descubrimos que, aunque todos los pacientes convalecientes analizados tenían títulos de anticuerpos positivos contra la proteína de superficie Spike cuando se midieron mediante ensayos de inmunoabsorción ligado a enzimas (ELISA), los niveles de anticuerpos neutralizantes contra el SARS-CoV-2 vivo fueron muy bajos en los individuos convalecientes y, por lo tanto, no lo hicieron. no aumentar los niveles de anticuerpos ni mejorar la progresión de la enfermedad en los receptores. Este estudio destacó la importancia de realizar un cribado previo del plasma de convalecencia no solo para detectar anticuerpos totales mediante ELISA, sino también para neutralizar los títulos de anticuerpos antes de la infusión en los pacientes. También hemos colaborado con TriCore Reference Laboratories para demostrar que los títulos de anticuerpos neutralizantes se correlacionan con un ensayo de detección de anticuerpos simple y rápido de uso comercial que no requiere el uso de virus vivos.
- Métodos de inactivación de SARS-CoV-2 en superficies.
Hemos probado varios métodos químicos, de calor, de luz y otros para inactivar el SARS-CoV-2 vivo. También hemos demostrado que un método comúnmente sugerido para descontaminar las máscaras N95 con calor seco no es efectivo para eliminar el SARS-CoV-2 vivo.
- Análisis de respuestas longitudinales de anticuerpos y linfocitos T en individuos convalecientes COVID-19. Recientemente hemos sido financiados por UNM HSC CTSC para rastrear las respuestas inmunes en pacientes después de su recuperación de la infección por SARS-CoV-2. Tenemos un IRB aprobado para este trabajo y actualmente estamos reclutando a 50 pacientes para analizar sus respuestas de anticuerpos y células T durante un período de hasta 10 años. Este trabajo responderá preguntas vitales sobre cuánto tiempo los sobrevivientes de COVID-19 tienen respuestas inmunes contra el virus.
- Cribado in vitro de moléculas pequeñas frente al SARS-CoV-2.
Uno de los aspectos principales de mi trabajo sobre el SARS-CoV-2 se centra en probar moléculas pequeñas para determinar su eficacia in vitro contra virus vivos en el laboratorio BSL-3. Hemos trabajado con UNM HSC, el campus principal de UNM e instituciones que no pertenecen a UNM para probar sus medicamentos para detectar actividad antiviral. Mi laboratorio ha analizado muchas moléculas pequeñas y ha encontrado unas pocas que inhiben de forma potente la replicación. Este trabajo ha dado lugar a muchas subvenciones, así como manuscritos en preparación o enviados, una muestra de los cuales se enumera a continuación.